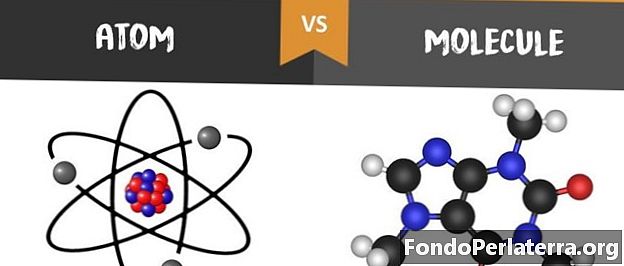
Atom vs. molekula

Obsah
- Obsah: Rozdíl mezi atomem a molekulou
- Srovnávací tabulka
- Co je Atom?
- Co je Molecule?
- Klíčové rozdíly
- Vysvětlení videa
Hlavní rozdíl mezi atomem a molekulou spočívá v tom, že atom je tvořen neutrony, protony a elektrony, zatímco molekula označuje skupinu atomů, které jsou spojeny kovalentní vazbou nebo iontovým kovem.
Obsah: Rozdíl mezi atomem a molekulou
- Srovnávací tabulka
- Co je Atom?
- Co je Molecule?
- Klíčové rozdíly
- Vysvětlení videa
Srovnávací tabulka
| Základ rozlišování | Atom | Molekula |
| Definice | Atom označuje nejmenší částici prvků, která obsahuje vlastnosti prvku | Molekuly označují skupinu atomů nebo kombinaci atomů |
| Závislost | Může nebo nemusí | Ano |
| Vlastnosti hmoty | Může nebo nemusí | Ano |
| Klasifikace | Ne | Dva: homomatický a heteroatomový |
| Síla | Základní stavební kameny hmoty | Více molekul v lidském těle než hvězdy ve vesmíru |
| Existence | Nemůže existovat samostatně | Může existovat nezávisle |
| Příklady | Kyslík, vodík a dusík | H2, NO atd. |
Co je Atom?
Atom označuje nejmenší částicovou jednotku jednoduché hmoty, která má vlastnosti chemického prvku. Všechny typy plynů, pevných látek, kapalin a plazmy jsou složeny z ionizovaných nebo neutrálních atomů. Obvykle jsou velmi malé a nelze je vidět skrze pouhé oči a zvětšovací mikroskop. Velikost atomu může být asi deset miliard miliard metru. Mluvím o jejich hranicích, pak ty nemají přesně definované hranice.
S postupným vývojem fyziky, atomové modely včlenily kvantové principy vysvětlit lepší a předpovídané chování atomu. Každý atom složený z jednoho nebo více elektronů je vázán na jádro.
Jádro atomu je vyrobeno z jednoho nebo více protonů a obvykle má podobný počet neutronů. Jádro atomu je také obklopeno elektrony, které jsou záporně nabité částice. Atom může být negativně nebo pozitivně nabit v závislosti na většině částic. Když se tyto záporné nebo kladné atomy spojí dohromady za vzniku molekul, vytvoří se vazby elektrony, které vyplňují vnější oběžné dráhy atomů. V atomu neexistuje vazba, protože atomy existují nezávisle.

Co je Molecule?
Molekula je nejmenší částice elektricky neutrální skupiny, která obsahuje chemické vlastnosti této sloučeniny nebo prvku. Jsou tvořeny atomy, které jsou drženy pohromadě chemickými vazbami. Tito jsou úplně odlišeni od iontů kvůli nedostatku elektrického náboje.
Atomy většiny chemikálií se rychle spojí s jinými atomy za vzniku molekul. Ty se mohou lišit velikostí a složitostí. Ty zůstávají vždy v pohybu. V tekutinách a pevných látkách jsou pevně zabaleny. V pevném stavu lze jejich pohyb přirovnat k rychlým vibracím. V kapalném stavu se tyto pohybují volně mezi sebou jakýmkoli způsobem klouzání. V plynném stavu je jejich hustota menší ve srovnání s pevnou a kapalnou látkou stejné chemické vazby a pohybuje se ještě volněji ve srovnání s kapalinou.
Ve srovnání s atomem má molekula schopnost sama o sobě existovat, a to díky elektronu přítomnému v atomu. V molekule může být atom stabilní pouze v případě dostupnosti dostatečného počtu elektronů. Podle Kinetic Theory of Gasses „molekula se často používá pro jakoukoli plynnou částici bez ohledu na její složení. Kvůli monoatomické molekulární struktuře jsou atomy vzácných plynů také považovány za molekuly. “

Klíčové rozdíly
- Atom je nejmenší částice prvku, zatímco molekula je nejmenší částice sloučeniny.
- Atom může nebo nemusí existovat nezávisle, zatímco molekula vždy existuje nezávisle.
- Atom může nebo nemusí mít vlastnosti hmoty, zatímco molekula má vždy vlastnosti hmoty.
- Molekuly jsou složeny z atomů atom je tvořen neutrony, protony a elektrony.
- Atom může být molekula díky nezávislé existenci. Atomy jsou přítomny v monoatomické molekule kvůli faktorům stability, jako jsou ušlechtilé plyny a helium, zatímco molekula nemůže tento atom říci.
- Atomy nemají žádné další druhy, zatímco molekuly mají dva typy, které jsou homomatickými molekulami a heteroatomickými
- Atomy nemají vůbec žádnou vazbu, zatímco molekuly mají mezimolekulární síly a intramolekulární
- Uspořádání atomů lze vidět pomocí rentgenového záření, zatímco v molekulách interakce umožňuje člověku pohybovat se, cítit, reprodukovat a spoustu dalších věcí.
- Tři různé typy atomu jsou atom vodíku, atom deuteria a tritium. Dva typy molekuly jsou jednoduchá molekula a komplexní molekula.
- Atom nemůže existovat nezávisle, zatímco molekula může existovat nezávisle.
- Atom prvku nemůže žít ve svobodném stavu, zatímco molekuly mohou žít ve svobodném stavu.
- Hmotu atomu nelze prakticky určit, zatímco součet hmotností jednotlivých atomů představuje hmotnost molekuly.
- Atomy mohou získat a ztratit elektrony za vzniku iontů, zatímco molekuly nemohou získat nebo ztratit elektrony za vzniku iontů.
- Je nemožné vidět atom pouhým okem a dokonce ani zvětšovacím obrazem. Molekulu také nelze vidět pouhým okem, ale lze ji vidět pomocí vysoce zvětšovacího mikroskopu.
- Atom nelze dále dělit, zatímco molekulu lze dále dělit na jednotlivé atomy.
- Atom má jadernou přitažlivost nebo spojení s ním, zatímco molekula má chemickou přitažlivost nebo propojení mezi atomy.